突破物理极限:光学超分辨成像技术的第一性原理与技术演进
突破物理极限:光学超分辨成像技术的第一性原理与技术演进
人类探索微观世界的历史,本质上是一部与“光的衍射性质”不断博弈的历史。自17世纪安东尼·范·列文虎克(Antonie van Leeuwenhoek)用简单的单透镜显微镜首次观察到微生物以来,光学显微镜一直是生命科学和材料科学不可或缺的工具。然而,随着研究的深入,科学家们撞上了一堵看似坚不可摧的物理叹息之墙——阿贝衍射极限(Abbe Diffraction Limit)。
1873年,Ernst Abbe提出了著名的衍射极限公式,宣告光学显微镜的分辨率上限约为 $\lambda/2NA$——对于可见光($\lambda \approx 500nm$)和高数值孔径物镜($NA \approx 1.4$),这一极限约为 200nm。
这一”物理铁律”统治光学显微学界超过一个世纪,直到2014年,Eric Betzig、Stefan Hell和William Moerner因突破衍射极限的超分辨荧光显微技术共同获得诺贝尔化学奖。他们的工作使光学显微镜的分辨率从200nm跃升至 20-30nm,开启了纳米尺度生物成像的新纪元。
本文将深入剖析两类主流超分辨技术的核心原理:受激发射损耗显微镜(STED) 与 单分子定位显微镜(PALM/STORM)。
第一章:阿贝衍射极限
要理解超分辨成像,必须首先理解我们为何会被“限制”。这种限制并非来自于透镜制造工艺的粗糙,而是深植于光作为一种电磁波的根本属性之中。
根据惠更斯-菲涅耳原理(Huygens-Fresnel principle),光在传播过程中,其波前的每一个点都可以看作是一个新的次波源。当光线穿过显微镜的圆形物镜光阑时,会发生衍射。这意味着,一个无限小的理想发光点(例如一个荧光分子),经过光学系统成像后,在像平面上并不会汇聚成一个无限小的点,而是形成一个中心明亮、周围有明暗相间同心圆环的衍射光斑——即艾里斑(Airy disk)。
核心差异对比摘要
为了更直观地理解,我们可以从以下几个维度进行对比:
| 对比维度 | 阿贝衍射极限 (Abbe) | 瑞利判据 (Rayleigh) |
|---|---|---|
| 物理视角 | 频域 (Fourier Optics) | 空域 (Image Space) |
| 理论模型 | 周期性光栅的衍射极值能否进入光瞳 | 两个独立点光源的艾里斑重叠程度 |
| 临界条件 | 至少捕获0级和一束1级衍射光 | 一个艾里斑主极大与另一个第一暗环重合 |
| 光场相干性 | 默认基于相干照明(光栅衍射) | 默认基于非相干照明(独立点光源强度叠加) |
| 数值公式 | $d = \frac{0.5 \lambda}{\text{NA}}$ | $d = \frac{0.61 \lambda}{\text{NA}}$ |
| 工程应用侧重 | 显微镜设计、光刻机分辨率、超构表面特征尺寸评估 | 望远镜分辨双星、单分子定位显微镜、光谱仪点云分辨 |
数值示例:
- $\lambda = 532nm$(绿光),$NA = 1.4$(油浸物镜)
- $d_{\min} \approx 190nm$
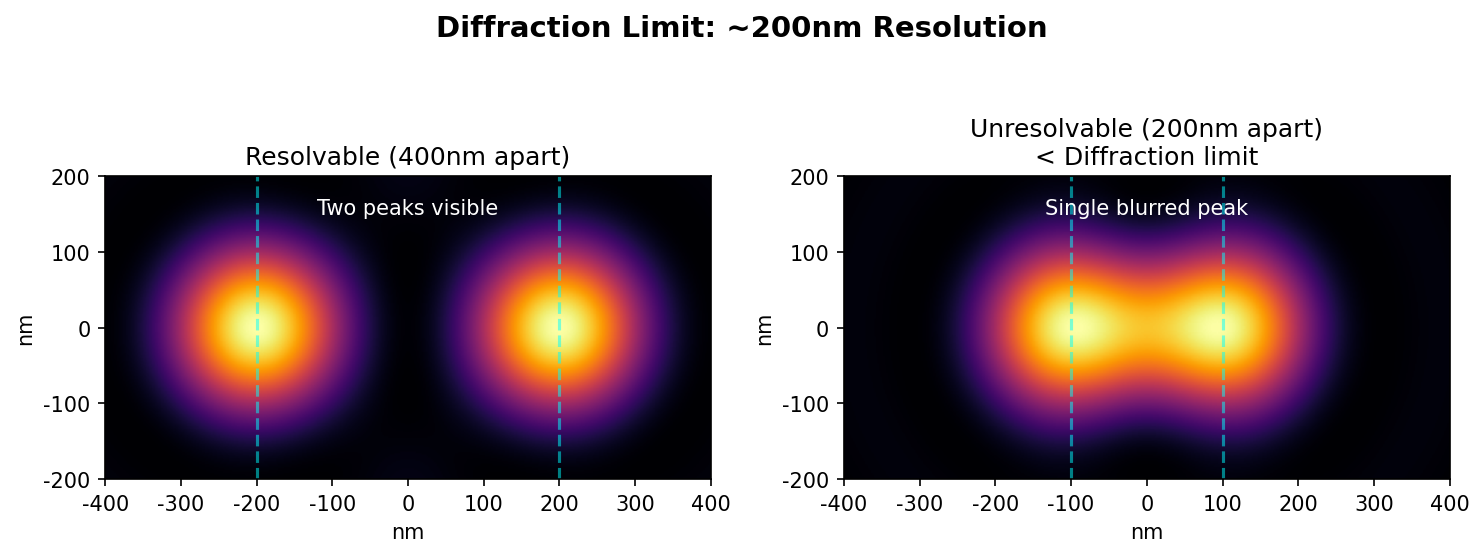
这意味着两个距离小于190nm的点无法被区分——它们会合并成一个模糊的光斑。
第二章:如何打破“不可打破”的法则?
当我们面临一个由物理定律限定的死胡同,第一性原理(First Principles)思考要求我们退回至最基本的事实,重新审视前提假设。
阿贝极限的假设前提是:所有发光点同时、持续地发光,且它们的发射光在空间中线性叠加。
如果这个前提不可动摇,那么在纯粹的空间域(Spatial Domain)和线性光学范畴内,阿贝极限确实是真理。因此,要打破极限,我们必须引入新的变量维度。历史给出的答案是:引入时间维度、非线性光与物质相互作用,或频域的非线性解调。
这就引出了超分辨成像的三大流派:
- 工程化PSF(空间非线性): STED (受激发射损耗显微术)
- 单分子定位(时间域多路复用): PALM / STORM
- 频域混合(信息论降维): SIM (结构光照明显微术)
第三章:时域、频域与量子态的博弈——核心技术解析
2014年,诺贝尔化学奖授予了Eric Betzig, Stefan W. Hell 和 William E. Moerner,以表彰他们在超分辨荧光显微技术领域的开创性贡献。以下我们将深入其物理内核。
3.1 STED:受激发射损耗显微术
Stefan Hell 提出的 STED (Stimulated Emission Depletion) 技术,可以说是对爱因斯坦于1917年提出的“受激辐射”理论的极致应用。
核心思想: 既然我们无法让激发光斑(PSF)变得更小,那我们就把发光斑周围的分子“强制熄灭”,只留下中心极小区域的分子发光。
物理机制:
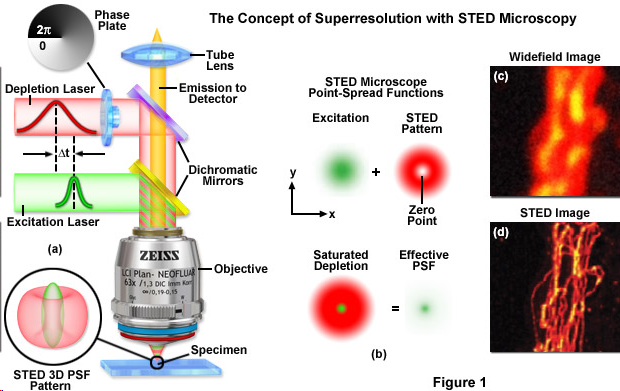
STED 系统使用两束激光:
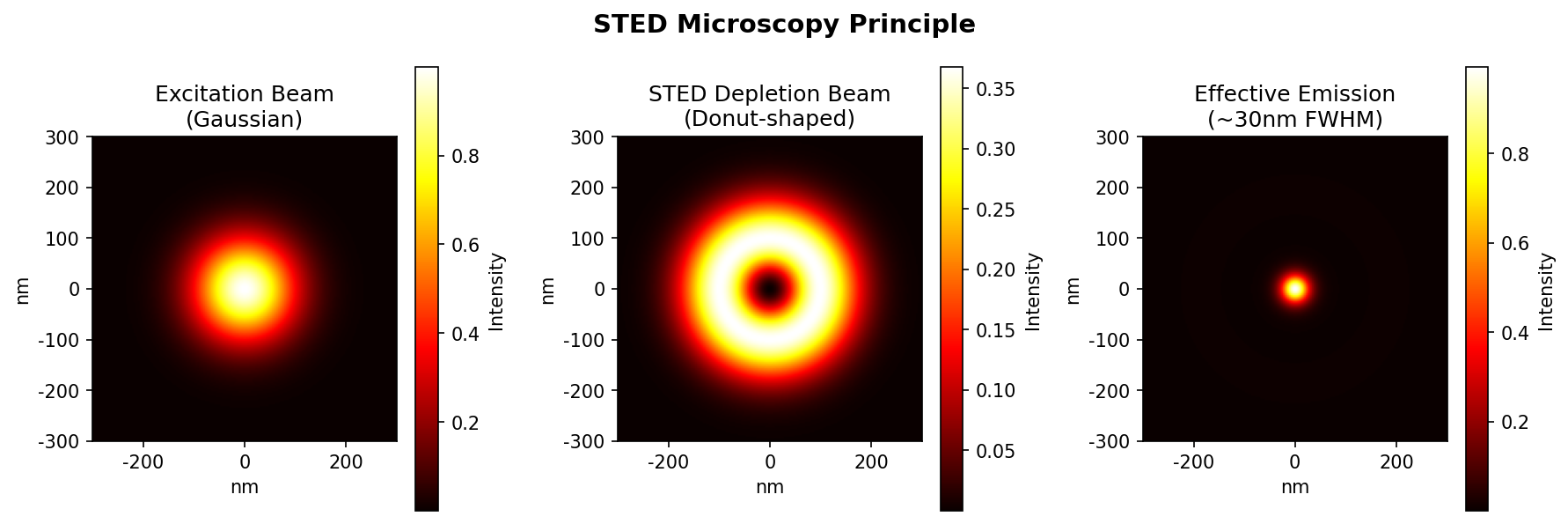
- 激发光(Excitation beam): 常规的高斯光束,激发衍射极限区域内的所有荧光分子。
- 损耗光(Depletion beam): 这是一束经过特殊相位调制的光,其中心强度为零,呈“甜甜圈”形状(Donut-shaped beam)。它的波长被设定在荧光分子发射光谱的红移尾部。
当损耗光照射到处于激发态的荧光分子时,会触发受激辐射(Stimulated Emission)。这种受激辐射过程极快,使得分子在自发辐射(发出我们想要的荧光)之前,就被“强制”打回基态,且释放的光子与损耗光同向同频,很容易被滤光片滤除。
由于“甜甜圈”中心的光强为零,位于正中心的分子不受损耗光影响,依然可以通过自发辐射发出荧光。通过无限增加损耗光的强度 $I$,可以无限压缩中心未被损耗的区域面积。
甜甜圈光束的实现原理
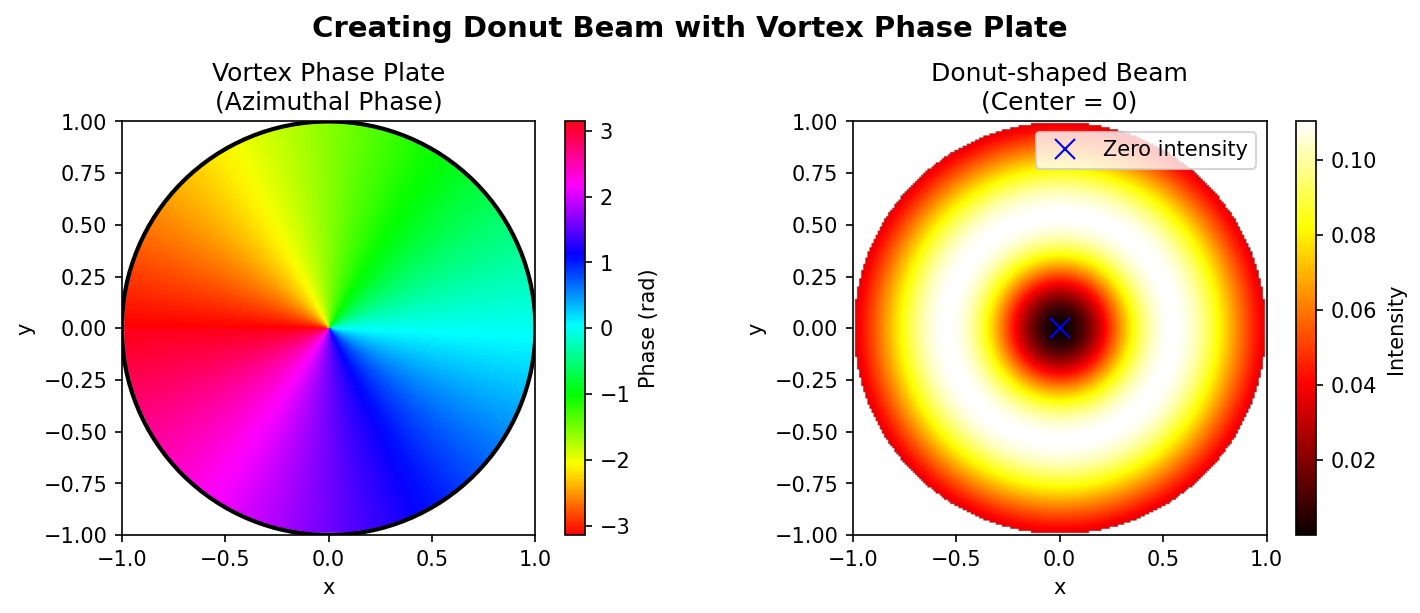
STED的关键创新在于使用涡旋相位板(Vortex Phase Plate) 生成甜甜圈形光束。
涡旋相位板的工作原理:
- 相位调制:涡旋相位板是一个特殊的透明光学元件,其厚度随方位角变化。当光束通过时,相位被空间调制:
$$
\phi(\theta) = l \cdot \theta
$$
其中 $l$ 是拓扑荷数(通常 $l=1$),$\theta$ 是方位角。
螺旋相位波前:经过相位板后,光束的波前从平面波变成螺旋形。在光束中心,所有方向的相位汇聚,导致相消干涉——中心光强为零。
傅里叶变换成像:物镜对螺旋相位光束进行傅里叶变换,在焦平面上形成环形光斑(甜甜圈形),中心暗、边缘亮。
数学推导:
对于拓扑荷 $l=1$ 的涡旋光束,焦平面上的电场分布为:
$$
E(r, \theta) = E_0 \cdot r \cdot e^{i\theta} \cdot e^{-r^2/w^2}
$$
光强分布:
$$
I(r) = |E|^2 = E_0^2 \cdot r^2 \cdot e^{-2r^2/w^2}
$$
关键特性:当 $r=0$ 时,$I(0) = 0$,即中心光强为零。
双光束配置与受激发射过程
STED使用两束同步激光:
| 光束 | 形状 | 波长 | 作用 |
|---|---|---|---|
| 激发光 | 高斯光斑 | 短波长(如532nm) | 将荧光分子从基态 $S_0$ 激发到激发态 $S_1$ |
| 损耗光 | 甜甜圈形 | 长波长(如592nm) | 通过受激发射强制外围分子返回基态 |
受激发射的物理过程:
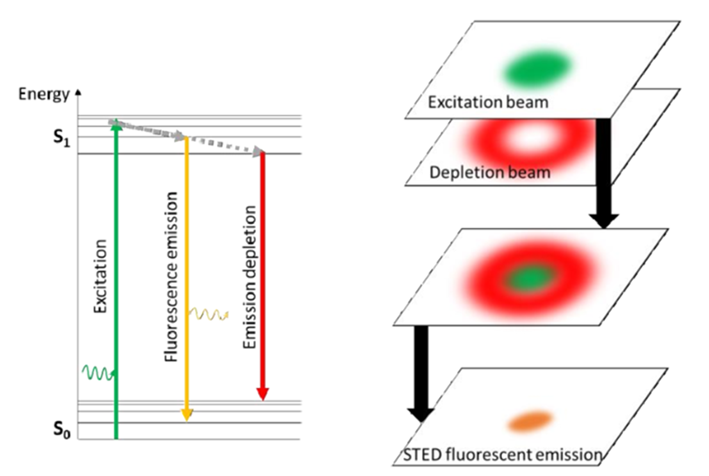
- 激发光将荧光分子激发到 $S_1$ 态
- 损耗光的光子能量恰好等于 $S_1 \to S_0$ 的能量差
- 当 $S_1$ 态的分子遇到损耗光光子时,会发生受激发射:分子被”诱导”发射一个与损耗光完全相同的光子,并返回基态
- 受激发射产生的光子波长与损耗光相同,可以被滤除,不会进入探测器
关键点:受激发射的速率与损耗光强度成正比。在甜甜圈外围,损耗光很强,受激发射概率接近100%;而在中心,损耗光为零,分子通过自发辐射发射荧光(我们想要的信号)。
有效PSF的数学推导
激发后的荧光分子处于激发态 $S_1$,可以通过两条路径返回基态:
- 自发辐射:发射荧光光子(我们想要的信号),速率 $\Gamma_{spont}$
- 受激发射:被STED光强制返回基态(被抑制),速率 $\Gamma_{STED} = \sigma \cdot I_{STED}$
其中 $\sigma$ 是受激发射截面,$I_{STED}$ 是损耗光强度。
留在激发态的概率(即可能发射荧光的概率):
`
$$
P_{fluor} = \frac{\Gamma_{spont}}{\Gamma_{spont} + \Gamma_{STED}} = \frac{1}{1 + I_{STED}/I_{sat}}
$$
其中 $I_{sat} = \Gamma_{spont}/\sigma$ 是饱和强度(荧光分子的特征参数)。
有效PSF变为:
$$
PSF_{eff}(r) = PSF_{exc}(r) \cdot \frac{1}{1 + I_{STED}(r)/I_{sat}}
$$
由于甜甜圈形损耗光在中心 $I_{STED}(0) = 0$、外围最强,中心区域的荧光被保留,外围被抑制。
有效发光区域的半径近似为:
$$
d_{STED} \approx \frac{\lambda}{2NA\sqrt{1 + I_{STED}^{max}/I_{sat}}}
$$
当 $I_{STED}^{max} >> I_{sat}$ 时,分辨率可以远低于衍射极限!
例如:$I_{STED}^{max}/I_{sat} = 100$ 时,分辨率可提高10倍,达到 ~20nm。
3.2 PALM / STORM:时间换取空间的统计学奇迹
如果说STED是物理学上的硬碰硬,那么PALM (Photoactivated Localization Microscopy) 和 STORM (Stochastic Optical Reconstruction Microscopy) 则是统计学与概率论在光学上的巧妙应用。
第一性原理: 如果两盏灯挨得很近同时亮起,我们无法分辨;但如果它们轮流闪烁,我们就能在不同的时间点精确定位它们各自的位置。
技术实现:
- 分子开关: 利用特殊的光致可转换(Photoswitchable)或光激活(Photoactivatable)荧光蛋白/染料。大多数时间它们处于暗态。
- 稀疏激活: 用极弱的特定波长激光照射样本,由于概率分布,只有极少数(空间上彼此分离、距离大于阿贝极限)的分子被随机激活发光。
- 高斯拟合定位: 虽然拍到的依然是模糊的艾里斑,但因为我们确信这个光斑只来源于单个分子,我们就可以求出这个光斑的强度中心(质心)。根据大数定律和统计学原理,只要收集到的光子数足够多,中心定位的精度可以远高于衍射极限。
数学表达:
单分子定位的精度 $\Delta x$ 主要受限于收集到的光子数 $N$ 以及背景噪声。其简化形式可表示为:
$$\Delta x \approx \frac{s}{\sqrt{N}}$$
其中 $s$ 是显微镜 PSF 的标准差。只要单个分子发出的光子数 $N$ 足够大(例如 $N=10000$),定位精度就可以提升两个数量级(如达到 $2nm$)。
经过数万次“激活-拍照-淬灭”的循环,系统收集了数百万个单分子的精确坐标,最终用这些坐标点“点彩画”般地重建出超高分辨率的图像。这是一种典型的以时间分辨率(采集需要数分钟甚至更久)换取空间分辨率的策略。
3.3 SIM:频域的摩尔纹密码
SIM (Structured Illumination Microscopy) 是从信息论和傅里叶光学的角度解决问题的典范。
核心逻辑: 显微镜的物镜就像一个低通滤波器(Low-pass filter),高频空间信息(即细微的结构细节)无法通过。SIM 巧妙地利用了摩尔纹(Moiré fringes) 效应。
物理机制:
当两个高频(细密)的图案叠加时,会产生一个低频(粗大)的拍频条纹(摩尔纹)。
在SIM中,我们用带有已知高频条纹的结构光(Structured Light)去照明样本。样本自身未知的高频细节(原本由于衍射极限无法进入物镜)与照明光的高频条纹发生干涉混合,产生了低频的摩尔纹。
这个低频摩尔纹携带着样本的高频信息,顺利通过了物镜的低通滤波!
随后,在计算阶段,通过改变结构光的相位和方向,拍摄多张图像。利用傅里叶变换将图像转换到频域:
传统线性SIM通常能将分辨率提高两倍(达到约 $100nm$),因为照明光本身的条纹细度也受衍射极限限制。但由于其无需极高的激光强度,且成像速度相对较快,SIM 成为活细胞超分辨成像的首选工具。
第四章:跨学科视角的深刻洞察
技术的发展从来不是孤立的。光学超分辨率技术的演进,深刻体现了经济学原理与科学哲学的交织。
在经济学中有“蒙代尔-克鲁格曼不可能三角”,在软件工程中有CAP定理。显微成像领域同样存在一个严酷的光毒性-分辨率-速度(Phototoxicity - Spatial Resolution - Temporal Resolution)不可能三角。
信息论告诉我们,获取信息是需要付出能量代价的。
- STED 获得了极高的空间分辨率和较快的速度,但其代价是使用了极高能量的损耗光束,这对于活细胞而言是致命的(光漂白和光毒性)。
- PALM/STORM 获得了最高的空间分辨率,且单次激发能量较低,但付出了极大的时间代价(需要拍摄数万张图像),完全无法捕捉活细胞内高速运动的细胞器。
- SIM 在三者之间取得了一种中庸的平衡。
没有一种技术是完美的,科研人员实际上是在进行一种“信息带宽”的分配博弈,根据生物学问题的具体需求,在空间细节、时间动态和系统生命力之间寻找帕累托最优(Pareto Optimality)。
参考文献:
Abbe, E. (1873). “Beiträge zur Theorie des Mikroskops und der mikroskopischen Wahrnehmung.” Archiv für Mikroskopische Anatomie, 9, 413-468.
DOI: 10.1007/BF02956173Betzig, E., Patterson, G. H., Sougrat, R., Lindwasser, O. W., Olenych, S., Bonifacino, J. S., et al. (2006). “Imaging intracellular fluorescent proteins at nanometer resolution.” Science, 313(5793), 1642-1645.
DOI: 10.1126/science.1127344Rust, M. J., Bates, M., & Zhuang, X. (2006). “Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM).” Nature Methods, 3(10), 793-795.
DOI: 10.1038/nmeth929Hell, S. W. (2007). “Far-field optical nanoscopy.” Science, 316(5828), 1153-1158.
DOI: 10.1126/science.1137395Reuss, M., Engelhardt, J., & Hell, S. W. (2010). “Birefringent device converts a standard scanning microscope into a STED microscope that also maps molecular orientation.” Optics Express, 18(2), 1049-1058.
DOI: 10.1364/OE.18.001049Xu, K., Zhong, G., & Zhuang, X. (2013). “Actin, spectrin, and associated proteins form a periodic cytoskeletal structure in axons.” Science, 339(6118), 452-456.
DOI: 10.1126/science.1232251Sigal, Y. M., Zhou, R., & Zhuang, X. (2018). “Visualizing and discovering cellular structures with super-resolution microscopy.” Science, 361(6405), 880-887.
DOI: 10.1126/science.aau1044Zeiss Microscopy Education. “STED Concept - Stimulated Emission Depletion Microscopy.”
https://zeiss-campus.magnet.fsu.edu/tutorials/superresolution/stedconcept/indexflash.html知乎专栏. “受激发射损耗(STED)显微镜原理.”
https://zhuanlan.zhihu.com/p/17032816386袁景和, 师锦涛(中科院化学所). “模块化受激辐射损耗(STED)显微镜.” 知乎专栏.
https://zhuanlan.zhihu.com/p/578120758OFweek光学. “STED显微技术介绍和应用.”
https://optics.ofweek.com/2024-06/ART-250003-11000-30638248.html《物理学报》. “超分辨显微成像技术在细胞器相互作用研究中的应用.” 物理学报, 2022, 51(11).
https://www.researching.cn/ArticlePdf/m00018/2022/51/11/20220622.pdf知乎专栏. “超高分辨显微镜在神经科学中的应用.”
https://zhuanlan.zhihu.com/p/605065079